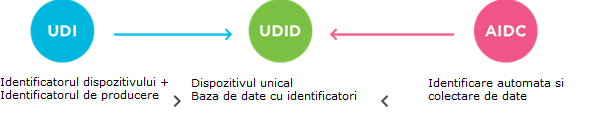
Administratia pentru Alimente si Medicamente SUA (FDA) , Comisia Europeana si alte organisme de reglementare au facut siguranta pacientilor o prioritate strategica in cautarea unei abordari armonizate la nivel global prin elaborarea Regulilor UDI pentru dispozitive medicale si de diagnostic in Vitro (IVD)
Regulamentil UE UDI privind identificarea a dispozitivelor medicale din 5 aprilie 2017.
Organizatia internationala GS1, saluta adoptarea a regulamentelor finale ale UE privind dispozitivele medicale si diagnosticarea in-vitro. Standardele globale GS1 vor fi utilizate de catre producatori pentru implementarea noului sistem UE de identificare a dispozitivelor unice (UDI), care vizeaza sprijinirea sigurantei pacientilor si a securitatii lantului de aprovizionare.
UDI si GS1
Organizatiile membre a GS1 sunt acele organizatii care emit GS1 Prefixe de companie (GCP) pentru a genera chei de identiificare GS1. De asemenea, ofera suport direct pentru utilizarea standardului GS1 pentru a implementa cerintele UDI in intreaga lume.
Sistemul de standarde GS1 ofera o baza conceptuala globala pentru identificarea, colectarea si publicarea informatiilor despre produse medicale, asigurand astfel realizarea a dispozitivelor medicale la nivel international.
GS1 a elaborat o noua cheie de identificare GMN (Numarul de Model Global) pentru a sprijini implementarea UDI-DI.
Pe site-ul GS1, puteti genera un GMN (UDI-DI de baza) , puteti calcula perechea de caractere pentru verificare corespunzatoare sau puteti verifica GMN.
Identificarea Unicala a produselor medicale in limbajul GS1
| UDI Identificarea unicala a dispozitivelor medicale |
Standarde GS1 Identificarea produselor |
| UDI-DI De baza Nivel «nou» de identificare in UE |
GMN (Nmarul de Model Global) Fara identificator de aplicatie (AI) pentru dispozitive medicale reglementate |
| UDI-DI * Identificatorul dispozitivului (DI) |
GTIN * Numarul Global a obiectului de vinzare |
| UDI-PI * Identificatorul producerii (PI) (daca se utilizeaza) |
AI * Identificatorul de Aplicatie (AI)
|
| Datele identificatorului de producere se vor deosebi in dependenta de tipul produselor medicale si regula de lucru a producatorului concret. | Datele identificatorului de producere se vor deosebi in dependenta de tipul produselor medicale si regula de lucru a producatorului concret. |
| UDI-DI + UDI-PI = UDI | GTIN или GTIN + AI(s) = UDI |
| * Formatul informatiilor care pot fi citite de om trebuie sa respecte regulile organizatiei care emite UDI. | * Formatul informatiilor care pot fi citite de om trebuie sa respecte regulile organizatiei care emite UDI. |
UDI in SUA
GS1 US Healthcare Supplier FDA UDI Ghidul rapid
Ghidul de implementare GS1 in SUA – Aplicarea sistemului de standarde
Exemple de etichete UDI, conforme cu cerintele FDA din SUA
UDI in UE
EUDAMED- Baza de date normativa a UE pentru dispozitive medicale
Intrebari frecvente Comisiei Europene referitor la codurile UDI
Mai multe informatii pe site-ul GS1