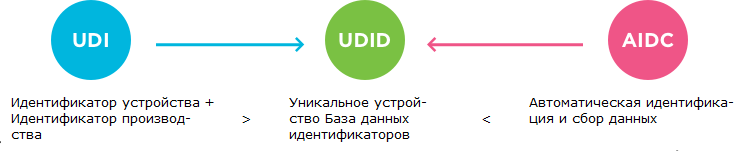
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), Европейская комиссия и другие регулирующие органы сделали безопасность пациентов стратегическим приоритетом и, стремясь к согласованному решению на глобальном уровне, разработали Правила UDI для медицинских устройств и устройств для диагностики in vitro (IVD).
Регламент EC UDI по идентификации медицинских устройств от 5 апреля 2017 года.
Международная организация GS1 приветствует сегодняшнее принятие окончательных Правил ЕС UDI по медицинским устройствам и in-vitro диагностике. Глобальные стандарты GS1 будут использоваться производителями для внедрения новой системы Уникальной Идентификации Устройств (UDI), которая направлена на обеспечение безопасности пациентов и цепи поставок.
UDI и GS1
Организации-члены GS1 – это те организации , которые выдают префиксы компаний GS1 (GCP), позволяющие генерировать идентификационные ключи GS1. Они также обеспечивают прямую поддержку использования стандарта GS1 для реализации требований UDI во всем мире.
Система GS1 стандартов обеспечивает глобальную концептуальную основу для выявления, сбора и публикации информации о продукте здравоохранения, тем самым обеспечивая последовательную реализацию медицинских устройств на международном уровне.
GS1 разработала новый ключ для поддержки реализации базового UDI-DI: GMN — Глобальный Номер Модели
На сайте GS1 вы можете сгенерировать GMN (базовый UDI-DI), вычислить соответствующую пару контрольных символов или проверить ваш GMN.
Уникальная Идентификация медицинских изделий на языке GS1
| UDI Уникальная идентификация медицинских устройств |
GS1 Стандарты Идентификация товаров |
| Базовый UDI-DI «Новый » уровень идентификации в EC |
GMN (Глобальный Номер Модели) Для идентификации медицинских устройств ИП не применяются |
| UDI-DI * Идентификатор устройства (DI) |
GTIN * Глобальный Номер Торговой Единицы |
| UDI-PI * Идентификатор производства (PI) (если применим) |
AI * Идентификатор Применения (AI)
|
| Данные идентификатора производства будут различаться в зависимости от типа медицинского устройства и текущей практики производителя. | Данные идентификатора производства будут различаться в зависимости от типа медицинского устройства и текущей практики производителя. |
| UDI-DI + UDI-PI = UDI | GTIN или GTIN + AI(s) = UDI |
| * Формат человекочитаемой информации должен соответствовать правилам организации, выдающей UDI. | * Формат человекочитаемой информации должен соответствовать правилам организации, выдающей UDI. |
UDI в США
GS1 US Healthcare Supplier FDA UDI Краткое руководство
Руководство по внедрению GS1 в США – Применение системы стандартов GS1 для уникальной идентификации устройств (UDI) FDA США
Примеры этикеток UDI, соответствующих требованиям FDA США
UDI в ЕС
Часто задаваемые вопросы Европейской комиссии по UDI
Узнать больше можно на сайте международной организации GS1